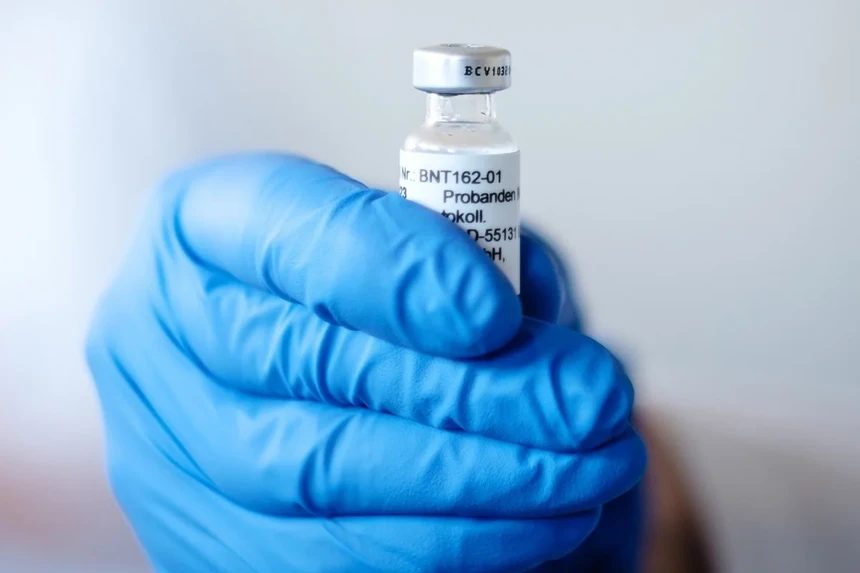
BioNTech cho biết trong một thông cáo báo chí rằng, nếu giấy phép được cấp thì vắc xin của Pfizer và BioNTech có thể sử dụng ở Châu Âu trước cuối năm 2020.
“Vì lợi ích của sức khỏe cộng đồng, người nộp đơn có thể được cấp phép tiếp thị có điều kiện cho những loại thuốc như vậy khi lợi ích của việc có sẵn ngay lập tức lớn hơn nguy cơ dữ liệu kém toàn diện hơn mức bình thường được yêu cầu. Tuy nhiên, người nộp đơn phải có khả năng cung cấp dữ liệu lâm sàng toàn diện trong tương lai”, EMA cho biết.
“Thông báo của ngày hôm nay đánh dấu một cột mốc quan trọng khác trong nỗ lực thực hiện lời hứa của chúng tôi là làm mọi thứ có thể để giải quyết cuộc khủng hoảng nghiêm trọng này do nhu cầu sức khỏe cộng đồng quan trọng”, tiến sĩ Albert Bourla, Chủ tịch và Giám đốc điều hành Pfizer cho biết trong thông cáo báo chí.
“Chúng tôi đã biết ngay từ đầu rằng các bệnh nhân đang chờ đợi và chúng tôi sẵn sàng vận chuyển các liều vắc xin Covid-19 ngay khi có sự cho phép tiềm năng”, tiến sĩ Albert Bourla cho biết.
Tin tức được đưa ra gần 2 tuần sau khi Pfizer và BioNTech cho biết rằng phân tích dữ liệu cuối cùng từ thử nghiệm lâm sàng giai đoạn cuối đối với vắc xin Covid-19 của họ cho thấy hiệu quả 95% trong việc ngăn ngừa lây nhiễm Covid-19.
Các nhà sản xuất thuốc cho biết vào giữa tháng 11, vắc xin được gọi là BNT162b2, có hiệu quả cao chống lại virus trong vòng 28 ngày sau liều đầu tiên, và hiệu quả của vắc xin là nhất quán ở mọi lứa tuổi, chủng tộc và sắc tộc.
Ngoài ra, những người cao tuổi, những người có nguy cơ mắc bệnh nặng do Covid-19 cao hơn, đã thấy hiệu quả của vắc xin hơn 94%, các công ty cho biết.
Pfizer và BioNTech đã nộp đơn xin cấp phép sử dụng khẩn cấp từ Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ cho vắc xin Covid-19 vào ngày 20/11, với quy trình của FDA dự kiến sẽ mất vài tuần và một cuộc họp của ủy ban tư vấn để xem xét vắc xin dự kiến vào đầu tháng 12.
Bên cạnh việc đệ trình lên EMA, Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) và Cơ quan Quản lý Thuốc và Sản phẩm Chăm sóc sức khỏe Vương quốc Anh (MHRA), BioNTech hôm thứ Ba (1/12) đã lưu ý rằng họ và Pfizer “đã bắt đầu đệ trình luân phiên trên toàn cầu, bao gồm cả ở Úc, Canada, Nhật Bản, và có kế hoạch gửi đơn trình lên các cơ quan quản lý khác trên thế giới”.
Nhà sản xuất dược phẩm Moderna hôm thứ Hai (30/11) cũng cho biết, họ sẽ nộp đơn xin cấp phép lên FDA và cơ quan tương đương ở châu Âu (EMA) sau khi dữ liệu mới xác nhận vắc xin này có hiệu quả hơn 94% trong việc ngăn ngừa Covid-19 và an toàn.